Une stratégie nouvellement proposée pour améliorer sensiblement les performances des batteries au lithium-soufre
Des chercheurs ont mis au point un médiateur d'oxydoréduction (redox) du soufre pour améliorer la cinétique de réaction lente de la batterie au lithium-soufre, qui a limité la densité énergétique de la batterie.
Les batteries au lithium-soufre sont très prometteuses en tant que dispositifs de stockage d'énergie de la prochaine génération en raison de leur densité d'énergie théorique très élevée. Cependant, la densité d'énergie réelle des batteries au lithium-soufre est loin de la valeur théorique en raison des graves limitations de la cathode dues à la lenteur des réactions d'oxydoréduction (redox) du soufre. L'équipe de recherche a créé une stratégie de médiation redox qui est efficace et qui propulse les batteries au lithium-soufre vers une application pratique.
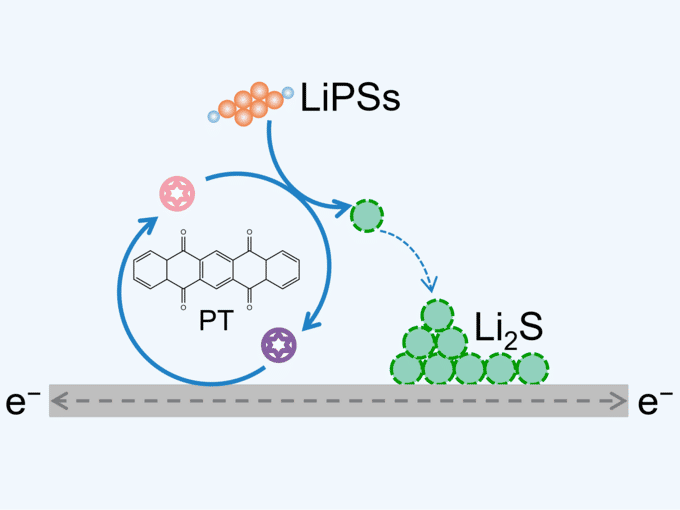
Les scientifiques ont créé un médiateur redox efficace pour promouvoir la cinétique redox du soufre dans des conditions de travail pratiques.
Nano Research, Tsinghua University Press
Les batteries au lithium sont largement utilisées aujourd'hui dans des applications allant de l'électronique portable aux véhicules électriques en passant par les systèmes de stockage d'énergie à l'échelle du réseau. Parmi les différentes batteries au lithium, les batteries lithium-ion sont devenues les plus populaires. Cependant, les batteries lithium-ion approchent de leur limite théorique de densité énergétique et ne peuvent pas répondre à la demande de dispositifs de stockage d'énergie à haute densité énergétique.
Les batteries au lithium-soufre, avec leur très haute densité d'énergie théorique de 2600 Wh kg-1, attirent une grande attention, comme alternative possible aux batteries au lithium-ion. Outre leur potentiel de haute densité énergétique, le soufre utilisé comme matière active dans la cathode est naturellement abondant, respectueux de l'environnement et peu coûteux.
Cependant, il reste un obstacle important à surmonter. La haute densité d'énergie théorique des batteries lithium-soufre provient des réactions entre la cathode de soufre et l'anode de lithium. Pendant le processus de décharge, lorsque l'énergie chimique est convertie en énergie électrique, le soufre est réduit en polysulfures de lithium dissous, puis en sulfure de lithium solide. Mais pendant ce processus de conversion, la cinétique, c'est-à-dire la vitesse des réactions chimiques, est très lente. Cette lenteur serait sérieusement aggravée dans des conditions de travail difficiles.
Pour résoudre le problème de la lenteur de la cinétique, les chercheurs ont conçu divers promoteurs pour améliorer les réactions de la batterie. Ces promoteurs servent d'hôtes de soufre ou de matériaux intercouches dans les batteries lithium-soufre et sont conçus pour favoriser la cinétique des batteries. Cependant, même avec ces promoteurs, les performances de la batterie diminuent progressivement en raison des dépôts solides de sulfure de lithium qui s'accumulent sur les sites actifs électrocatalytiques.
Après une étude plus approfondie, les chercheurs ont déterminé que les médiateurs redox solubles sont efficaces pour promouvoir la cinétique. Redox, abréviation d'oxydation-réduction, décrit les réactions chimiques qui se produisent. Ces médiateurs redox réduisent ou oxydent chimiquement les polysulfures de lithium, puis se régénèrent à la surface de l'électrode. Les chercheurs ont prouvé que l'utilisation des médiateurs redox est un mécanisme efficace pour résoudre le problème de la cinétique lente des piles bouton. Les piles à pièces, également appelées piles boutons, sont de petites piles plates utilisées dans de petits appareils tels que les appareils auditifs, les clés de voiture ou les implants médicaux. Il fallait ensuite trouver un médiateur redox qui fonctionne dans les piles au lithium de type poche, qui sont utilisées dans des applications de plus grande puissance, comme les applications militaires et automobiles.
L'équipe de recherche a estimé qu'il était urgent de mettre au point un médiateur redox avancé adapté aux piles au lithium-soufre à poche. L'équipe de recherche a donc conçu un médiateur redox utilisant une molécule organique appelée 5,7,12,14-pentacènetétrone, ou PT, pour promouvoir la cinétique redox du soufre dans les cellules à poche de lithium-soufre à haute densité énergétique. "Concrètement, le médiateur redox PT fournit une dérivation chimique pour la réduction du polysulfure de lithium en sulfure de lithium, ce qui réduit la résistance à la réaction et améliore la capacité de dépôt", a déclaré Bo-Quan Li, chercheur universitaire à l'Institut de technologie de Pékin. Les travaux de l'équipe fournissent un médiateur redox efficace pour la réduction du polysulfure avec une cinétique rapide et vérifient le potentiel d'application des médiateurs redox avancés dans les batteries lithium-soufre pratiques à haute densité énergétique.
Pour l'avenir, la prochaine étape des chercheurs consistera à développer des médiateurs redox plus avancés pour une régulation complète de la cinétique redox du soufre à la cathode. Avec ces médiateurs avancés, l'anode en lithium métal serait protégée, soit par la conception de l'électrolyte, soit par l'introduction d'hôtes en lithium. "L'objectif ultime est de réaliser des batteries lithium-soufre à haute densité énergétique et à long cycle, à faible coût et très sûres. Les applications potentielles de ces batteries lithium-soufre pourraient être les véhicules aériens et les engins spatiaux", a déclaré M. Li.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.