Nouvelles connaissances sur la décomposition de l'ammoniac
Comment rendre l'hydrogène transportable
L'utilisation de l'Ammoniac est considérée comme une méthode prometteuse de transport de l'hydrogène. Toutefois, un processus efficace est également nécessaire pour le reconvertir en hydrogène et en azote.
Une équipe de recherche internationale a acquis de nouvelles connaissances sur le mode de fonctionnement d'un catalyseur à base de fer qui peut être utilisé pour diviser l'ammoniac en azote et en hydrogène. L'hydrogène est converti en ammoniac pour faciliter le transport du vecteur énergétique. Cela signifie qu'il faut également des catalyseurs capables de décomposer l'ammoniac en ses matières premières. Une équipe de l'université allemande de la Ruhr à Bochum, du Max Planck Institute for Chemical Energy Conversion (MPI CEC) à Mülheim an der Ruhr, de la Technische Universität Berlin et de l'Italian Institute of Technology à Gênes décrit en détail comment le catalyseur à base de fer permet cette réaction dans la revue ACS Catalysis à partir du 6 septembre 2024.
Comment rendre l'hydrogène transportable
L'hydrogène vert est considéré comme un vecteur énergétique prometteur. Il peut être produit en séparant l'eau à l'aide de l'énergie éolienne ou solaire. Cependant, dans de nombreux cas, les lieux où l'hydrogène est nécessaire n'offrent pas les conditions adéquates pour l'électrolyse de l'eau. L'hydrogène doit être liquéfié pour être transporté, ce qui n'est possible qu'à des températures extrêmement basses. La conversion de l'hydrogène en ammoniac, qui peut être liquéfié à des températures beaucoup plus élevées, est donc considérée comme une alternative intéressante. "De plus, l'industrie chimique dispose déjà d'une infrastructure bien établie pour le traitement de l'ammoniac", explique le professeur Martin Muhler, directeur du laboratoire de chimie industrielle de Bochum et titulaire d'une bourse Max Planck à la CEC MPI.
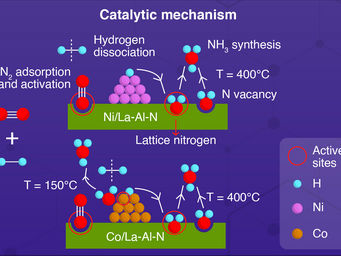
Des catalyseurs efficaces sont nécessaires pour décomposer l'ammoniac (NH3) en ses composés de départ, l'azote (N2) et l'hydrogène (H2). Le problème est que les catalyseurs conventionnels à base de fer facilitent généralement une réaction indésirable en formant du nitrure de fer au lieu de l'azote. Dans l'étude actuelle, les chercheurs ont montré exactement comment cette réaction secondaire se produit. Ils ont testé la décomposition de l'ammoniac à l'aide d'un catalyseur de dernière génération fourni par Clariant.
L'équipe composée du Dr Maximilian Purcel, d'Astrid Müller et du professeur Martin Muhler de l'université de la Ruhr à Bochum et du MPI CEC a réalisé les expériences correspondantes. Les résultats ont été affinés à l'aide de simulations complexes de dynamique moléculaire, soutenues par l'apprentissage automatique, qui ont été réalisées par l'institut partenaire italien. L'équipe de la Technische Universität Berlin a réussi à identifier les nitrures de fer formés dans les conditions de réaction à l'aide de la diffraction des rayons X et à suivre leurs transformations.
De futurs catalyseurs plus efficaces
"Nos résultats peuvent être utilisés pour développer des catalyseurs plus efficaces pour la décomposition de l'ammoniac à l'avenir", conclut Martin Muhler. "La synthèse et la décomposition de l'ammoniac ont une longue histoire", ajoute-t-il. "Nous citons des publications scientifiques datant des 100 dernières années. Parmi ces publications figurent les travaux de Gerhard Ertl, le directeur de thèse de Martin Muhler, qui a reçu le prix Nobel pour ses recherches en 2007.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.