Évolution de l'oxygène et du chlore sans métaux nobles
Le potentiel de l'électrode transforme les surfaces
Ils sont hautement sélectifs et peuvent être facilement séparés du mélange réactionnel : les catalyseurs à atome unique combinent les avantages de la catalyse homogène et de la catalyse hétérogène. Jusqu'à présent, leur production était généralement associée à des métaux précieux ancrés sur un substrat solide. Des chercheurs de l'université de Duisbourg-Essen viennent de montrer que de telles structures peuvent également être formées par voie électrochimique, indépendamment et sans métaux nobles. Leurs résultats, publiés dans la revue scientifique JACS*, ouvrent de nouvelles voies pour une production plus simple et plus durable de matériaux catalytiquement actifs.

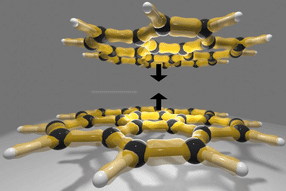
Un potentiel d'électrode appliqué transforme la surface du MXène : les atomes de métaux non nobles migrent vers l'extérieur et forment des "structures de type SAC" - des centres actifs pour l'évolution de l'oxygène ou du chlore gazeux.
© UDE/AG Exner
Les MXènes sont une classe de matériaux bidimensionnels qui n'ont été découverts qu'en 2011. Des études théoriques avaient prédit qu'ils ne seraient pas catalytiquement actifs dans les processus anodiques. Les chercheurs dirigés par le professeur Kai S. Exner, directeur du département de catalyse théorique et d'électrochimie de l'université de Duisbourg-Essen (UDE), viennent de réfuter cette théorie à l'aide d'une modélisation à plusieurs échelles.
Les scientifiques ont découvert que lorsqu'un potentiel d'électrode est appliqué, la surface du MXène se transforme en une structure en forme de brosse : les atomes de métaux non nobles migrent vers l'extérieur et forment ce que l'on appelle des "structures de type SAC" (single atom catalyst-like). Ces catalyseurs servent de médiateurs pour deux réactions importantes, à savoir l'évolution de l'oxygène et l'évolution du chlore.
Il en résulte un matériau dont la surface présente des sites catalytiques actifs sans ajout de métaux précieux. Nous avons conclu que les MXènes se comportent de la même manière que les enzymes dans un environnement électrochimique : en appliquant un potentiel d'électrode, leurs sites actifs sont créés directement dans le processus", explique Exner.
L'équipe a également pu montrer que les structures de type SAC qui en résultent sont sélectives : si de l'eau et des ions chlorure se trouvent en même temps dans l'environnement de la réaction, seul du chlore gazeux est formé. La formation de ce produit chimique de base est un processus clé dans l'industrie chimique, qui produit plus de 70 millions de tonnes de chlore gazeux (Cl2) par an. Le Cl2 est nécessaire à la production de produits pharmaceutiques, de plastiques, de batteries et au traitement de l'eau. Toutefois, lorsque l'électrolyte ne contient que de l'eau, la surface active du MXène facilite la production d'oxygène gazeux (O2) par évolution de l'oxygène - une étape importante dans la formation d'hydrogène vert dans un électrolyseur.
Cette découverte peut grandement simplifier la production de catalyseurs à un seul atome. L'élimination des métaux précieux coûteux permet également de réduire les coûts et les dépendances.
Des chercheurs de l'université de Barcelone (Espagne) et des scientifiques de Ruhr Explores Solvation (RESOLV) ont également participé à l'étude. RESOLV est un pôle d'excellence de l'Alliance universitaire de la Ruhr.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.