Des catalyseurs deux cent fois meilleurs grâce au carbone
"Pendant longtemps, l'utilisation du carbone comme matériau porteur pour la catalyse a eu quelque chose de presque magique"
Annonces
Lorsque l'on place des nanoparticules métalliques sur du carbone, elles deviennent beaucoup plus actives. Ce qui n'était auparavant qu'une hypothèse basée sur l'expérience a pu être expliqué en détail pour la première fois à l'Université technique de Vienne (TU Wien).

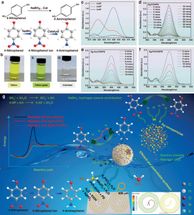
Une minuscule nanoparticule d'argent (atomes réfléchissants sur le dessus) sur un support de carbone. La zone limite (marques colorées) est celle où l'activité est la plus élevée.
Technische Universität Wien

L'équipe : Günther Rupprechter, Andreas Steiger-Thirsfeld, Michael Stöger-Pollach, Alexander Genest, Thomas Wicht, Thomas Haunold. (de gauche à droite)
Technische Universität Wien


Les métaux précieux jouent un rôle important dans l'industrie chimique en tant que catalyseurs : Grâce à l'argent, au platine, au palladium ou à d'autres éléments, des réactions chimiques peuvent avoir lieu alors qu'elles n'auraient pas lieu autrement ou qu'elles n'auraient lieu qu'à un taux de réaction beaucoup plus faible. Ces métaux sont souvent utilisés sous la forme de minuscules nanoparticules. Toutefois, leur efficacité dépend également de la surface sur laquelle elles sont placées. Les nanoparticules placées sur une base de carbone semblent particulièrement efficaces, mais la raison en est restée longtemps inconnue.
À la TU Wien, cependant, il a été possible pour la première fois de mesurer précisément et d'expliquer l'interaction entre les nanoparticules métalliques et un substrat de carbone. Les atomes d'argent sur un support de carbone se sont révélés deux cents fois plus actifs que les atomes d'un morceau d'argent pur. Les simulations informatiques montrent que la zone dans laquelle l'argent est en contact direct avec le carbone est cruciale. Grâce à l'échange d'isotopes d'hydrogène, une méthode a été mise au point pour tester plus rapidement et plus facilement l'efficacité des supports de catalyseurs.
De l'art noir à la science
"Pendant longtemps, l'utilisation du carbone comme matériau de support pour la catalyse a eu quelque chose de presque magique", explique le professeur Günther Rupprechter de l'Institut de chimie des matériaux de l'Université technique de Vienne (TU Wien). La source du carbone s'est avérée importante. Pour certains procédés, on utilise du carbone obtenu à partir de coquilles de noix de coco, de fibres ou de bois spéciaux. De telles "recettes" peuvent même être trouvées dans des documents de brevet - bien que l'origine des substances chimiques soit en fait relativement peu importante. "Cela a toujours ressemblé à de l'art noir", explique Günther Rupprechter.
L'idée était que les différentes méthodes de fabrication pouvaient entraîner des différences chimiques ou physiques minimes : peut-être le carbone s'arrange-t-il différemment selon la méthode de fabrication ? Peut-être contient-il des traces d'autres éléments chimiques ? Ou bien des groupes fonctionnels s'accumulent-ils à la surface - de petits éléments moléculaires qui interviennent dans la réaction chimique ?
"Dans l'industrie chimique, on se contente souvent du fait qu'un processus fonctionne et peut être répété de manière fiable", explique M. Rupprechter. "Mais nous voulions aller à l'origine de l'effet et comprendre exactement ce qui se passe au niveau atomique. L'université de Cadix (Espagne) et le centre de microscopie électronique USTEM de l'université technique de Vienne ont également participé à ces travaux.
Mesures de précision dans un microréacteur
L'équipe a d'abord produit des échantillons pouvant être caractérisés avec une extrême précision : des nanoparticules d'argent d'une taille connue sur un substrat de carbone - et une fine feuille d'argent sans carbone.
Les deux échantillons ont ensuite été examinés dans un réacteur chimique : "L'argent peut être utilisé pour diviser les molécules d'hydrogène en atomes d'hydrogène individuels", explique Thomas Wicht, premier auteur de l'étude. "Cet hydrogène peut ensuite être utilisé, par exemple, pour la réaction d'hydrogénation de l'éthène. De manière analogue, on peut également mélanger des molécules d'hydrogène "ordinaires" avec des molécules d'hydrogène lourd (deutérium). Les deux molécules sont alors dissociées par l'argent et recombinées". Plus le catalyseur est actif, plus les deux isotopes d'hydrogène sont échangés fréquemment. Cela fournit des informations très fiables sur l'activité du catalyseur.
Ainsi, pour la première fois, la différence d'activité entre les atomes d'argent avec et sans support de carbone a pu être quantifiée avec précision - avec des résultats spectaculaires : "Pour chaque atome d'argent, le support de carbone induit une activité deux cents fois plus élevée", explique Thomas Wicht. "C'est évidemment très important pour les applications industrielles. Il suffit d'un deux centième de la quantité de métaux précieux coûteux pour obtenir la même activité, et ce simplement en ajoutant du carbone comparativement peu coûteux".
L'effet excitant se produit à la frontière
Alexander Genest, de l'équipe de la TU Wien, a réalisé des simulations informatiques comparant l'activation de l'hydrogène par des nanoparticules d'argent sur du carbone et par de l'argent pur. Il en est ressorti clairement que la zone limite entre les particules d'argent et le support de carbone est cruciale. C'est exactement à l'endroit où les deux entrent en contact que l'effet catalyseur est le plus important. "Il ne s'agit donc pas de la taille de la surface de carbone, ni d'atomes étrangers ou de groupes fonctionnels. Un effet catalytique extrême se produit lorsqu'une molécule de réaction entre en contact avec un atome de carbone et un atome d'argent directement à l'interface", explique Alexander Genest. Plus cette zone de contact direct est grande, plus l'activité est importante.
Grâce à ces connaissances, il est désormais possible de vérifier facilement l'efficacité de différents lots de carbone provenant de différentes sources. "Maintenant que nous avons compris le mécanisme d'action, nous savons exactement à quoi nous devons faire attention", explique Günther Rupprechter. "Notre expérience, qui consiste à exposer les catalyseurs à un mélange d'hydrogène ordinaire et d'hydrogène lourd, est relativement facile à réaliser et fournit des informations très fiables sur la question de savoir si cette variante du support de carbone convient également à d'autres réactions chimiques. La possibilité d'expliquer les processus au niveau atomique devrait désormais permettre d'économiser du temps et de l'argent dans l'industrie et de simplifier l'assurance qualité.
Note: Cet article a été traduit à l'aide d'un système informatique sans intervention humaine. LUMITOS propose ces traductions automatiques pour présenter un plus large éventail d'actualités. Comme cet article a été traduit avec traduction automatique, il est possible qu'il contienne des erreurs de vocabulaire, de syntaxe ou de grammaire. L'article original dans Anglais peut être trouvé ici.